碳纳米纤维/聚己内酯/矿化羟基磷灰石纳米纤维支架的潜在骨科应用
2017-09-12 文章来源:丁悦 邱俊雄(中山大学孙逸仙纪念医院骨外科) 作者:丁悦 邱俊雄(中山大学孙逸仙纪念医院骨外科) 我要说
期刊年卷:Acs Applied Materials & Interfaces, 2017, 9(7):6342.
作者:Shinyjoy Elangomannan, Kavitha Louis, Bhagya Mathi Dharmaraj, Venkata Saravanan Kandasamy, Kannan Soundarapandian, and Dhanaraj Gopi
背景介绍
生物材料是有助于提高人类寿命和质量的物质,随着人均寿命的提高生物材料也在迅速发展。用于硬组织修复和替代的生物材料是一个挑战性且有前景的研究领域,尤其是在骨组织工程领域。通常,用于组织再生的材料都必须具有生物相容性表面以及良好的机械性能。考虑到机械性能、生物相容性及耐腐蚀性,钛植入物是用于各种骨骼锚固重建的最常用金属材料之一。然而,这些金属表面的生物活性普遍很低,故为了提高生物活性,需要对其进行表面处理以增强与骨组织之间的相互整合。
钛植入物通常涂覆有羟基磷灰石(HAP),一种与人类硬组织无机矿物具有相似化学及晶体学特性的生物陶瓷材料。这种钛植入物上的生物活性涂层有利于促进植入物与骨组织之间的整合。HAP是多矿物取代磷酸钙,可以进一步被各种矿物离子所取代,以增强生物学性质。为了提高材料的生物活性,取代的矿物须促进细胞附着和增殖以诱导骨再生。将锰替代进入HAP(Mn-HAP),有利于成骨细胞增殖并增加生物相容性。另外,由于镓对骨组织的强亲和力、抑制骨吸收及抗菌活性,其在生物医学应用领域也得到广泛应用。
虽然HAP和矿化的HAP(M-HAP)可诱导骨生长,但它们的机械性能较差,最常用的解决方法是在其中混入合适的多聚物。聚己内酯(PCL),一种半结晶脂肪族多聚物,是一种具有显着韧性、优异生物相容性、良好生物降解性、高机械强度、高断裂能的重要生物降解聚合物。此外,PCL易形成复杂的形状,具有良好的孔隙率。这些特性使PCL适合用于长期植入物。将HAP掺入多聚物基质中可获得与生物环境之间更好的相互作用及细胞粘附。
长期的高载荷会对这些多聚物/HAP复合材料的机械性能产生不利影响。机械性能较差,主要是由于HAP的脆性以及它与多聚物之间缺乏相互作用。为克服这个缺点,可在其中加入适当的增强材料,如碳纳米管(CNTs)、碳纳米纤维(CNF)、二氧化钛、二氧化锆等。在这些增强材料中,CNF价格便宜,毒性小,易功能化且较CNTs易分散,是一个很好的选择。CNF可提供额外的结构稳定性、良好的导电性及机械稳定性。功能化的CNF可形成各种化学键,进而改善其与HAP基质间的相容性。综上所述,CNF可大大改善复合材料的机械性能。
一般来说,用于骨组织再生的理想材料必须有良好的生物相容性、生物降解性、机械性能及简便的生产工艺。本文报道了一种纳米纤维支架(CNF/PCL/M-HAP)的研发及特性。CNF、PCL、M-HAP三者的组合可显着提高其耐腐蚀性、机械性能及生物相容性。因此,CNF/PCL/M-HAP纳米纤维支架可能会是一种合适的骨科材料。
相关方法及结果
1.红外光谱

对复合材料的形成过程中发生的结构改变进行傅里叶变换红外光谱分析。图1中诸如磷酸基、羟基、羧基等特征峰的存在证实了CNF/PCL/M-HAP复合纳米纤维支架的形成。
2.X射线衍射

对PCL/M-HAP以及混合不同浓度CNF的CNF/PCL/M-HAP复合材料进行X射线衍射。
在图2(b-d)中,CNF、PCL、M-HAP的特征峰表明CNF/PCL/M-HAP在钛金属上成功形成了复合涂层,同时CNF的加入也没有引起PCL/M-HAP涂层的明显结构变化。
3.高分辨率扫描电镜(HRSEM)和能谱分析(EDAX)

不同矿物取代的HAP以及PCL结合的矿物取代HAP的形态如图3(a-d)所示。锰取代HAP的HRSEM照片(图3a)显示了它们之间存在含有不规则孔隙的小颗粒。镓取代的HAP(图3b)呈现出高度分布均匀的粒子。PCL涂层的形态(图3c)形成群簇状结构。对于PCL/M-HAP涂层(图3d),PCL的典型群簇状结构仍然占主导地位,还可看到其他小颗粒。

图4(a-d)显示了不同CNF浓度(1%、2%、3%重量)的CNF/PCL/M-HAP复合涂层的HRSEM图像。图中可看到所有复合涂层均相互连接。图4(b)表明CNF(2%)均匀覆盖PCL和M-HAP。氧化的CNF具有足够的亲水性和许多官能团,M-HAP可以沿着CNF表面的PCL分子快速沉积在氧化的CNF上。

图5是包含2%CNF含量的CNF/PCL/M-HAP复合涂层的不同元素EDAX图

图6是不同CNF浓度复合涂层的透射电子显微镜(TEM)图像。CNF浓度为1%时复合材料呈现分散状;浓度提高至2%时管状的CNF周围存在很少颗粒,这可能代表了复合涂层中多聚物及矿物质取代HAP的存在;浓度为3%时纳米纤维表面会附着一些凝集颗粒。故在本研究中,CNF的最佳浓度为2%,可加强复合涂层的机械学及生物学特性。
4.电化学特性
4.1 电位极化研究
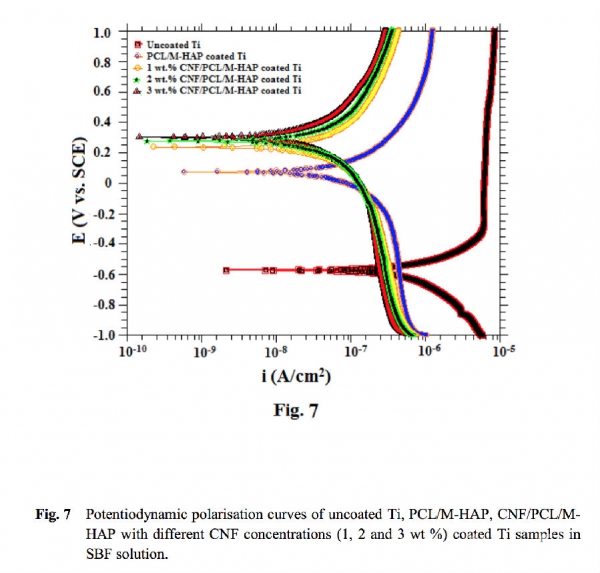
分别检测未涂覆及加涂层的钛金属在仿生模拟体液(SBF)的耐腐蚀能力。图7是未涂覆的钛,PCL/M-HAP、不同CNF浓度的CNF/PCL/M-HAP涂覆钛样本的电位极化曲线。图中显示2%CNF的CNF/PCL/M-HAP涂层可以作为防腐蚀阻挡层,并增加植入物负重耐力。
4.2 电化学阻抗光谱学研究(EIS)
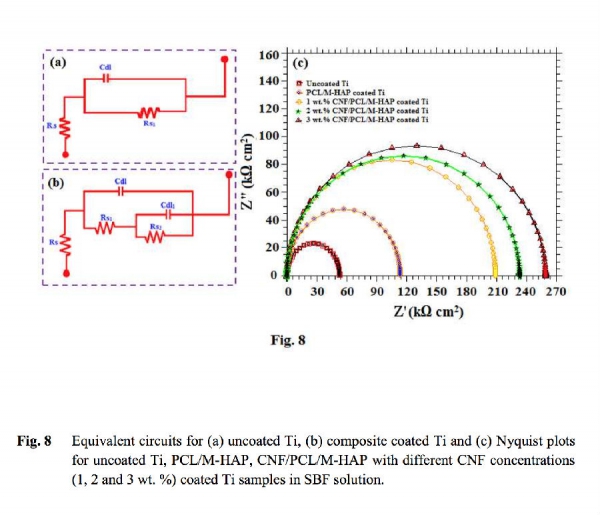
EIS是通过电化学阻抗曲线提供机械信息的主要方法之一。图8(a-b)分别是在SBF溶液中未涂覆、有复合涂层钛样本的代表性等效电路,图8(c)为EIS光谱。图中可以看出,在钛金属上的2%CNF的CNF/PCL/M-HAP复合涂层在具有优异的耐腐蚀性能,可延长骨科植入物的寿命。
5.涂层的机械学特性:粘附强度、维氏显微硬度
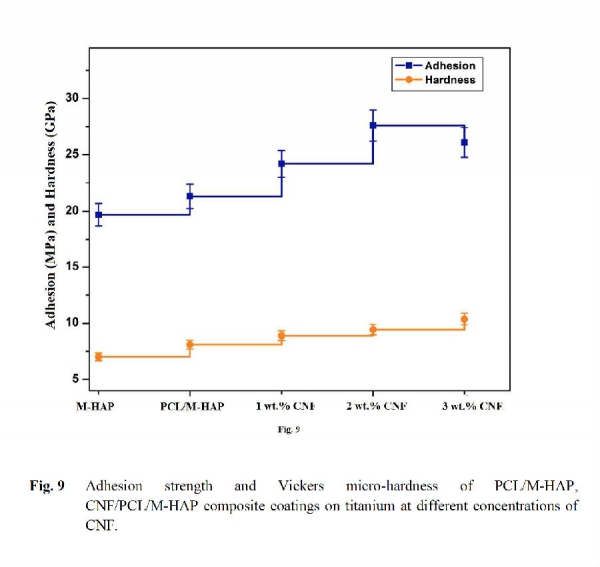
使用ASTM F 1044-05粘附试验检测不同涂层在钛金属上的粘附强度,结果如图9所示。2%CNF的CNF/PCL/M-HAP涂层具有最高的粘附强度。涂层中的CNF对钛金属表面具有优异的粘附力,这种高粘附强度将使得该材料非常适合于承重应用。
维氏显微硬度(Hv)是承重金属植入物的最重要参数。通过维氏显微硬度试验对几种材料进行测试,结果如图9所示。CNF的存在提高了钛金属表面涂层的硬度,使其适用于骨科承重。复合涂层钛金属的机械性能(粘附强度,弹性模量和硬度)与天然骨骼相当,其机械性能满足人类骨组织所需。
6.生物特性
6.1 抗菌活性
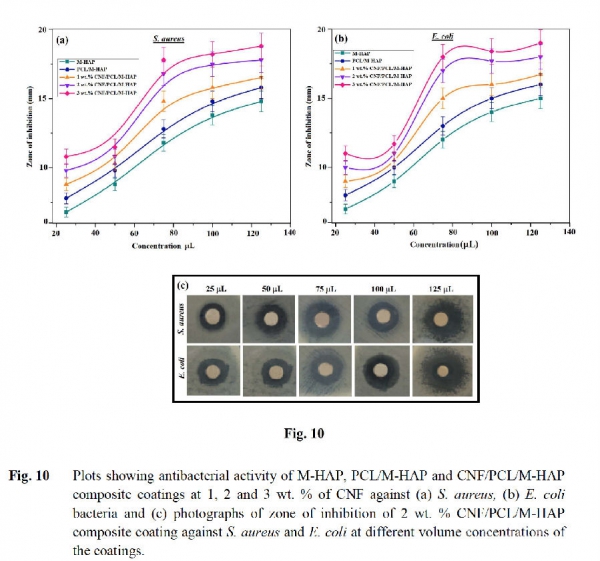
为避免手术感染,必须评估生物陶瓷涂层金属植入物的抗菌活性。使用光盘扩散法研究这几种复合材料对于大肠杆菌和金黄色葡萄球菌的抗菌活性(术后感染往往与这两种细菌相关)。图10显示复合涂覆样品在不同浓度下对金黄色葡萄球菌(图10a)和大肠杆菌(图10b)的抑制区。CNF/PCL/M-HAP复合涂层的抑菌区域均比其他样本大。复合材料中的抗菌活性得益于其中含有的镓离子及锰离子。
6.2 体外生物相容性
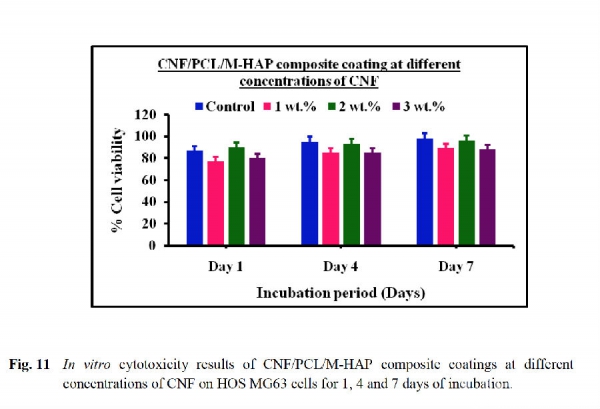
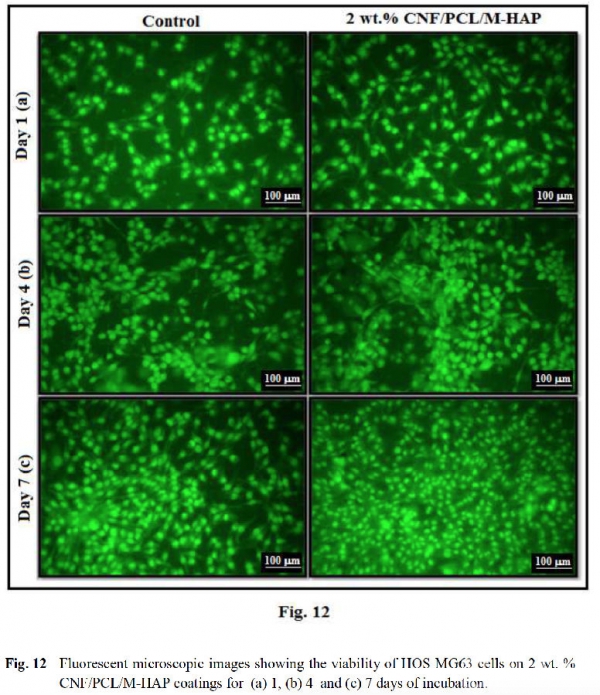
通过在不同孵育时间点的HOS MG63细胞MTT试验检测几种复合涂层的细胞毒性,图11显示所有涂层均明确无毒性,且CNF的最佳浓度为2%。图12是细胞在CNF (2%) /PCL/M-HAP涂覆的钛金属上孵育不同时间点的荧光显微镜图像,结果显示7天的孵育时间最适合细胞的粘附增殖。
6.3 体内生物相容性
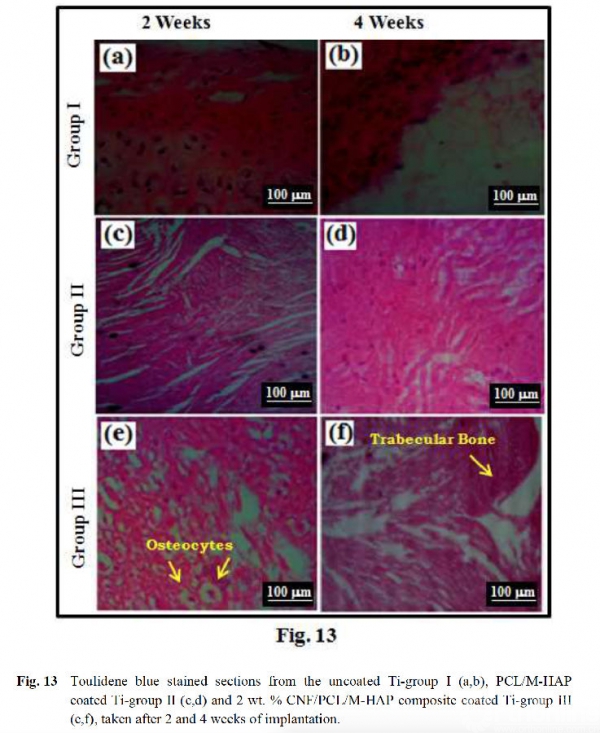
为了评估复合涂层植入物在体内的生物相容性,在雄性Wister大鼠股骨内植入无涂覆的钛金属、PCL/M-HAP涂层钛金属及CNF(2%)/PCL/M-HAP涂层钛金属。所有小鼠的手术部位均完全愈合,植入了复合涂层植入物的动物也迅速恢复。特别是植入CNF(2%)/PCL/M-HAP涂层钛金属(第III组)的小鼠在观察期间无任何感染迹象。组织学检查(图13)显示复合涂层钛植入物中无炎症发生。由新形成的小梁骨可以看出,III组CNF(2%)/PCL/M-HAP钛植入物表现出最好的愈合反应(图13f)。
结论
本研究旨在介绍一种新型的纳米纤维支架在骨科植入物中的潜在应用。不同浓度的CNF(1、2、3%重量)与M-HAP、PCL基质的混合使得其在物理化学、形态学、电化学、机械和生物学特性方面有很大的改善。我们通过红外光谱、X射线衍射、能谱分析、透射电子显微镜等方法明确证实了钛金属上CNF/PCL/M-HAP复合涂层的存在。在电化学特性中可看到复合涂层良好的耐腐蚀性。复合涂层中CNF的加入可改善多个方面的特性。随着CNF增加到某个特定浓度,复合材料的粘附强度和硬度也增加。MTT试验也证实了复合涂层表面成骨细胞的活力及增殖情况。从小鼠的体内实验可以看出,这种新材料可以使得植入物与骨组织直接结合。目前仍需进行其他大型动物的体内研究来评估CNF/PCL/M-HAP复合材料作为骨替代材料的前景。



 京公网安备11010502051256号
京公网安备11010502051256号