曹旭、罗卓荆教授团队联手揭开骨外膜干/祖细胞调控机制
2019-06-07 文章来源:空军军医大学西京医院骨科 我要说
骨科在线版权所有,如需转载请注明来自本网站.
骨外膜被附于除关节面外的皮质骨表面,含有丰富的神经与血管供应,对皮质骨的生长、修复和营养具有关键性调控作用。此外,骨外膜含有大量具有成骨分化及再生修复功能的干/祖细胞,为皮质骨的生长发育与再生修复提供源源不断的种子细胞。
然而,骨外膜为何具有强大的促成骨能力?骨外膜是否具有自身独特的“Periosteal Niche”?骨外膜干/祖细胞在皮质骨生长与再生修复过程中如何行使其功能?解决以上问题将加深大家对骨外膜这一关键结构的认知。
2019年5月20日,约翰霍普金斯医学院曹旭教授团队联合空军军医大学西京医院骨科罗卓荆教授团队在The Journal of Clinical Investigation上发表题为“Macrophage-lineage TRAP+ cells recruit periosteum-derived cells for periosteal osteogenesis and regeneration”的论著,发现骨外膜TRAP+细胞可持续募集骨外膜细胞到皮质骨表面,并参与骨外膜成骨微环境的构建,对皮质骨的生长与再生修复起到关键性调控作用。

曹旭教授与罗卓荆教授为通讯作者,高博主治医师为第一作者,Johns Hopkins邓若晛博士为共同第一作者
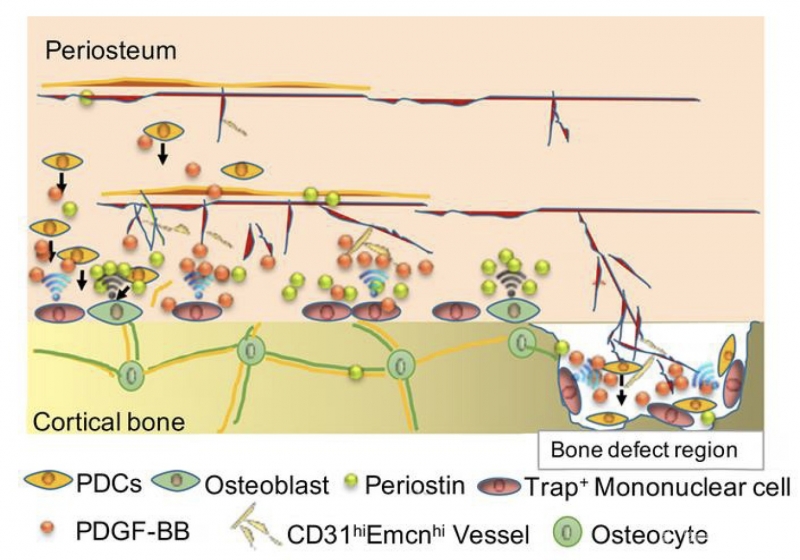
团队研究发现,骨外膜具有明显的双层结构,骨外膜内层含有丰富的H型血管内皮细胞以及骨膜素(Periostin),共同构建骨外膜独特的成骨微环境。在皮质骨生长与再生修复过程中,骨外膜Trap+细胞通过持续募集骨外膜干/祖细胞到皮质骨表面,并通过刺激分泌骨膜素,进一步促进细胞粘附于骨表面并向成骨方向分化。当巨噬细胞缺乏时,骨外膜微环境与结构受到显著影响,皮质骨形成障碍,提示Macrophage-lineage细胞对骨外膜niche的构建至关重要;然而,当Trap+细胞减少或功能缺失时,骨外膜干/祖细胞迁移受阻,同时骨外膜成骨微环境显著破坏,皮质骨形成与再生修复受到显著影响。
进一步研究发现,骨外膜Nestin+与LepR+细胞中含有部分干/祖细胞亚群,在皮质骨不同生长发育时期发挥作用,并参与骨外膜Niche的构建。
本研究通过系列研究,阐明了骨外膜TRAP+细胞在皮质骨形成与再生中的关键作用,并系统分析了不同时期骨外膜Nestin+与LepR+干/祖细胞亚群在皮质骨再生修复与骨外膜微环境构建中的作用。
团队简介
空军军医大学西京医院骨科罗卓荆教授团队长期从事脊柱退变、干细胞衰老与再生以及神经再生的基础研究与临床治疗工作,在相关领域取得丰硕的研究成果。
团队带头人罗卓荆教授
所获荣誉:国家科技进步二等奖1项、省部级科学技术一等奖1项、二等奖2项,荣获第16届吴阶平-保罗杨森医学药学奖。先后承担国家重点研究计划项目、973课题、军队医药卫生重点课题等项目研究工作。
学术任职:先后担任中国医师协会骨科医师分会常务委员,中国康复医学会脊柱脊髓专业委员会副主任委员,解放军骨科专业委员会副主任委员,陕西省医学会脊柱分会主任委员,陕西省医学会骨科学分会副主任委员,中国生物医学工程学会再生医学与组织工程分会副主任委员等。
团队近五年共发表SCI 论文46篇,包括:
The Journal of Clinical Investigation (IF:13.251)
PNAS (IF:9.8)
Biomaterials(IF:8.806)
Theranostics (IF:8.537)
Aging Cell (IF:7.627)
Acta Biomaterial (IF:6.383)
J Bone Miner Res (IF:6.314)
EBiomedicine (IF:6.183)
Cell Death and Disease (IF:5.965)
FASEB J (IF:5.596)等



 京公网安备11010502051256号
京公网安备11010502051256号