金大地教授团队新研究揭示高溶解性pH中性生物活性玻璃成骨成血管机制
2020-07-13 文章来源:骨科在线 我要说
临床上临界骨缺损通常需要借助骨修复材料来实现,主要包括自体骨、同种异体骨及合成生物材料等。自体骨仍然是“金标准”,但是来源有限,并且会造成新的创伤,增加患者痛苦。同种异体骨又存在疾病传播、免疫排斥反应等问题。因此,合成生物材料逐步进入人们的视野,并成为当前医用生物材料领域的研究重点。
生物活性玻璃是目前唯一不依赖外加生长因子而能体现骨诱导性的合成材料,有潜力媲美自体骨,但是它作为骨修复材料仍然不是完美的,至少需要改善两种特征:①在接触体液时会导致pH值明显升高,不利于细胞生长;②溶解度性较差,释放的骨诱导性关键离子(可溶性硅酸根离子)有限。因此,具有中性pH和较高溶解度的生物活性玻璃可能是更好的人工骨移植材料。
南方医科大学第三附属医院金大地教授与中国科学院化学研究所邱东教授研究团队,联合对新近开发的高溶解性pH中性生物活性玻璃(PSC)进行了系统考察,发现其在体外和体内均体现出更优异的骨修复特性并阐明了其机制。研究者认为该PSC生物玻璃具有良好的临床转化前景,可作为临床修复骨缺损的常规骨修复材料。相关论文在线发表在Materials Science and Engineering: C(DOI:10.1016/j.msec.2020.111249) 上。
众所周知,成骨和成血管特性是骨移植材料最重要的两个因素,具有协同促进这两种因素的骨修复材料将是非常理想的。与两种经典骨修复材料45S5生物活性玻璃和β-磷酸三钙(β-TCP)相比,PSC显著改善了BMSCs的增殖、迁移和矿化作用,并促进了成骨和成血管分化。在大鼠颅骨缺损中,PSC在诱导骨再生方面表现出比45S5和β-TCP更强的作用,骨密度升高和新生骨面积增加。与空白对照组相比,PSC显着促进了新生血管的形成。此外,我们还揭示了PSC通过PI3K / Akt /HIF-1α通路协同作用,研究中发现HIF-1α表达水平与P-Akt表达相一致。我们推测PI3K / Akt通路可能会影响与氧有关的代谢活动,进而调节氧含量和HIF-1α活性,促进BMSCs的成骨和成血管分化,这在以前未有报道。
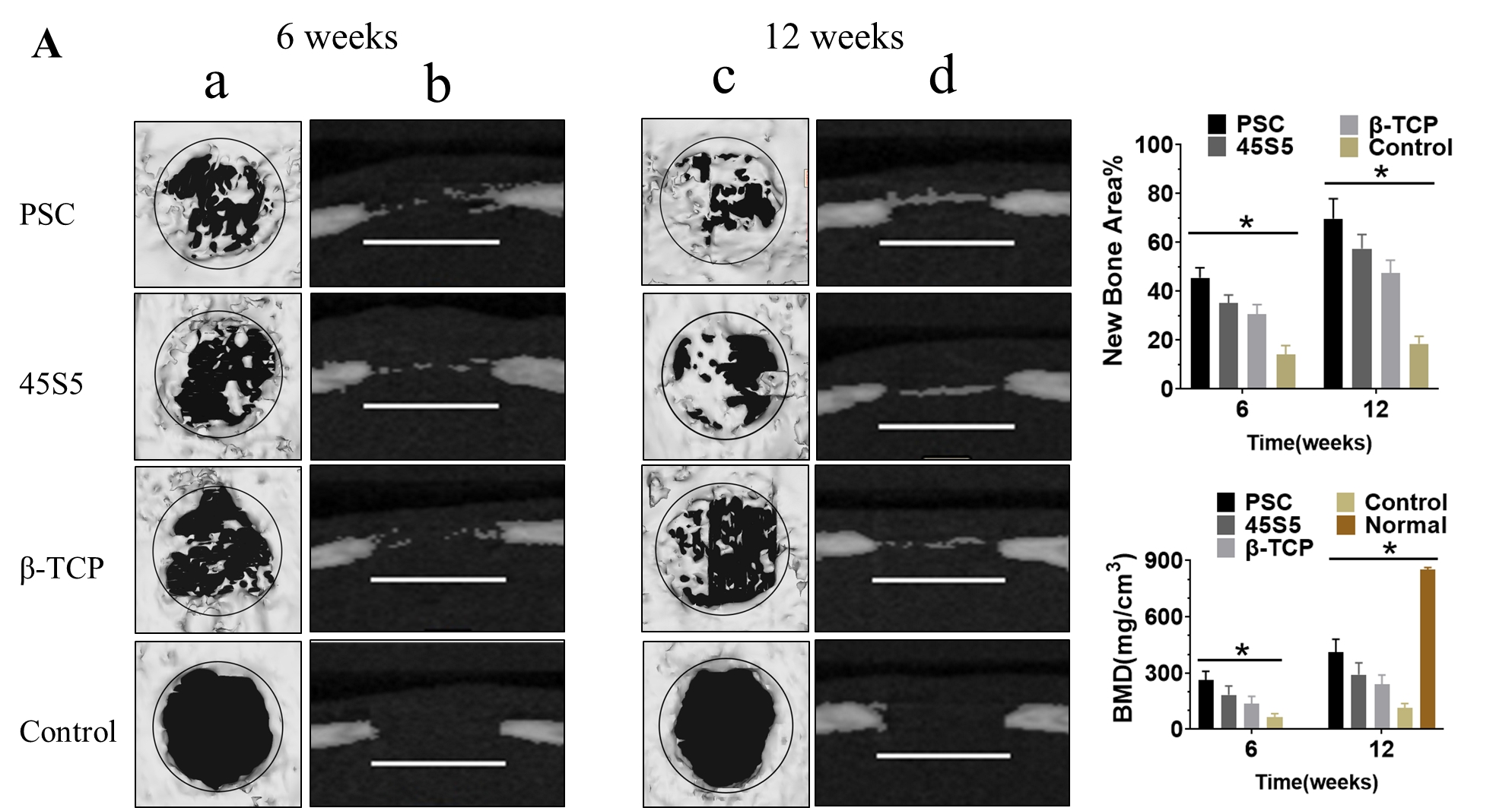
大鼠颅骨缺损的Micro-CT分析
A:Micro-CT显示大鼠颅骨的水平面(a,c)和冠状面(b,d)
B:新骨面积的统计结果
C:骨密度的统计结果。圆直径5mm,比例尺5mm
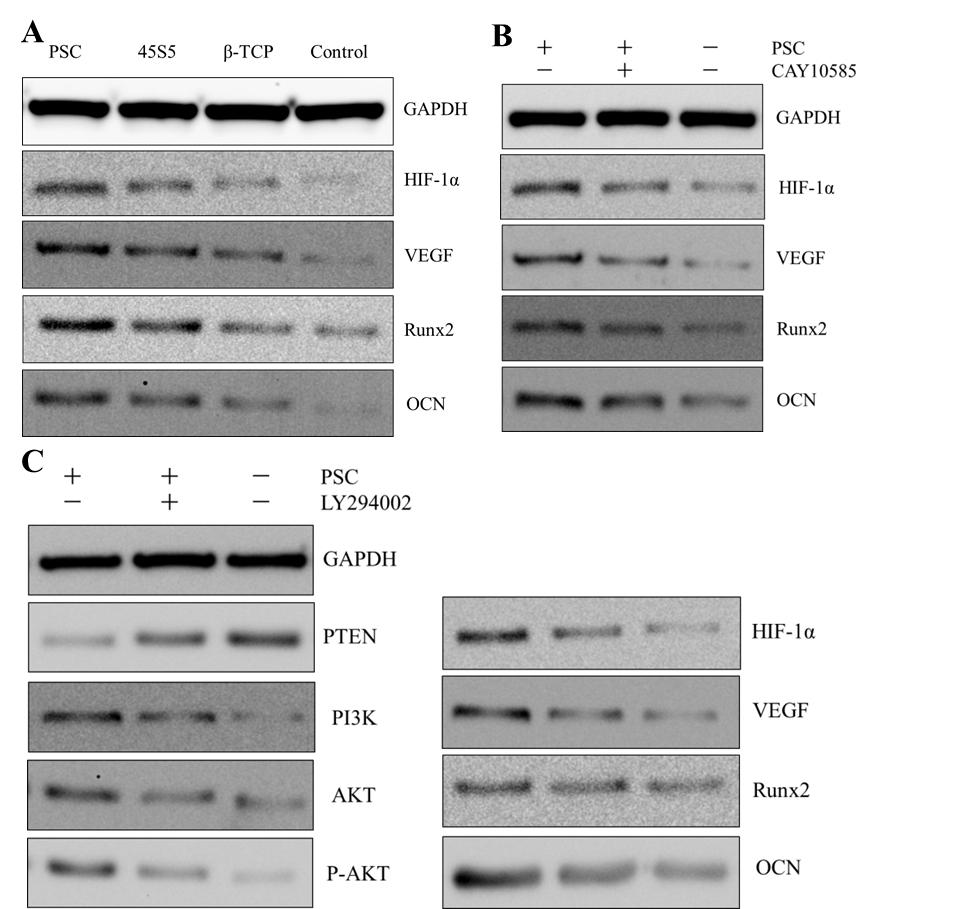
PSC,45S5和β-TCP对BMSCs成骨分化和成血管分化的影响以及PSC的作用机制
A)PSC,45S5和β-TCP对BMSCs成骨分化和成血管分化的作用
B:“”在有或没有HIF-1α抑制剂时,PSC对BMSCs中Runx2, OCN, HIF-1α 和VEGF蛋白水平的影响
C:在有或没有PI3K抑制剂时,PSC对BMSCs中PTEN, PI3K, Akt, P-Akt, Runx2, OCN, HIF-1α 和 VEGF蛋白水平的影响
来源:南方医科大学第三附属医院



 京公网安备11010502051256号
京公网安备11010502051256号